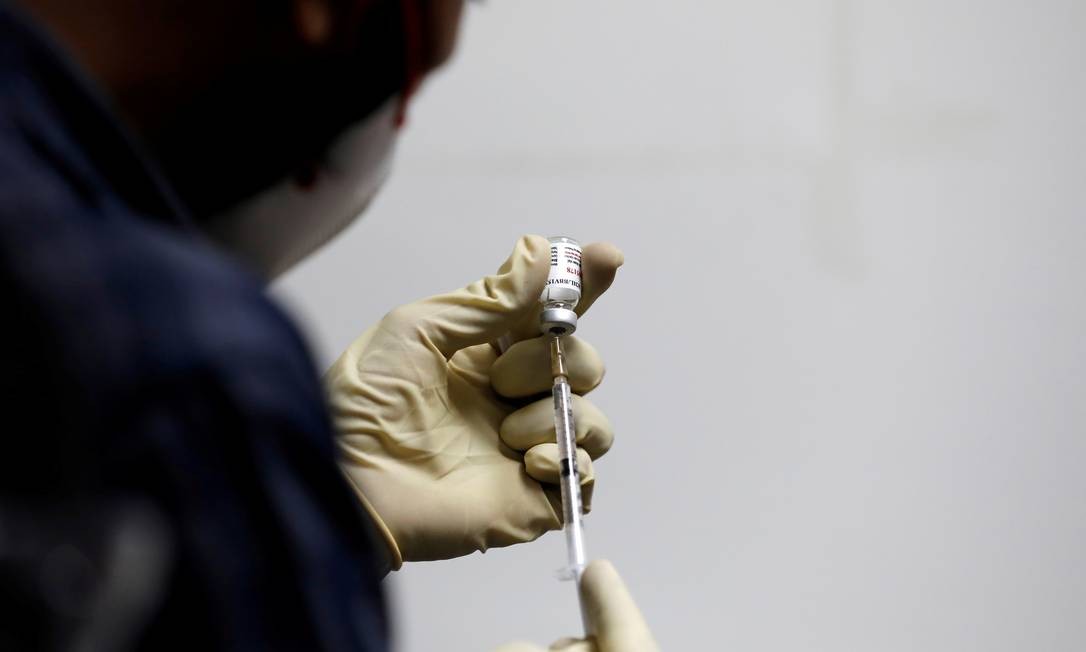
Médico segura uma seringa com Covaxin, imunizante indiano aprovado em seu país para uso emergencial este domingo (3) Foto: AMIT DAVE/REUTERS/26-11-2020
RIO - A Associação Brasileira das Clínicas de Vacinas (ABCVAC) informou neste domingo (3) que busca a importação de 5 milhões de doses do imunizante Covaxin, aprovado para uso emergencial na Índia contra a Covid-19.
A ABCVAC, cujas associadas representam 70% do mercado nacional, está negociando a compra com o laboratório indiano Bharat Biotech. A entrada do produto no mercado brasileiro dependeria de autorização da Agência Brasileira de Vigilância Sanitária.
Presidente da ABCVAC (Associação Brasileira das Clínicas de Vacinas), Geraldo Barbosa projeta oferta de imunizantes em clínicas particulares ainda em 2021
A aprovação emergencial da vacina na Índia, que ocorreu este domingo, foi criticada por especialistas, já que ela se encontra na fase 3 de pesquisas e sua taxa de eficácia não é conhecida. Até agora, porém, os estudos não demonstraram danos colaterais significativos.
Em entrevista à Globo News, Geraldo Barbosa, presidente da ABCVAC, afirmou esperar que os testes da vacina sejam concluídos na Índia ainda em janeiro. Se isso ocorrer, o laboratório deve entrar com pedido de registro definitivo na Anvisa em fevereiro, e a vacina pode estar disponível nas clínicas particulares brasileiras a partir da segunda quinzena de março.
Segundo Barbosa, ainda não há previsão do custo do imunizante, já que não há detalhes sobre a logística e distribuição do imunizante para o Brasil e as clínicas associadas. O presidente da ABCVAC destaca que a tecnologia do vírus inativo permite que o acondicionamento da vacina seja realizado entre 2 a 8 °C.
O presidente da ABCVAC destaca que a compra de vacinas por clínicas particulares não vai interferir na aquisição de imunizantes pelo poder público, ressaltando que a prioridade é o cumprimento do Plano Nacional de Imunização apresentado pelo governo federal.
— A gente já vem buscando saídas para o mercado privado e surgiu a possibilidade dessa vacina indiana, que é muito promissora. Como o mercado todo já estava comprometido com as demandas do governo – corretamente, porque eu acho que tem que ser prioridade –, a gente tentou uma saída alternativa — explicou Barbosa a Globo News. — E essa indústria indiana se disponibilizou a oferecer parte da produção para o mercado privado brasileiro. Então, é uma venda adicional que não vai interferir no quantitativo que o governo pediu.
Mellanie Fontes-Dutra, pesquisadora da Universidade Federal do Rio Grande do Sul, destaca que, em todo o mundo, a administração das vacinas tem sido realizada pelos governos — portanto, a entrada do setor privado neste processo pode ser "complicada". Outro fator potencialmente crítico é a falta de informações sobre a eficácia da Covaxin.
— Em breve conheceremos dados sobre a fase 3 da vacina, o número de eventos e o perfil dos pacientes: de que idade são, como é o seu fundo genético — explica.
De acordo com Barbosa, os dados sobre a Covaxin estão há cerca de 40 dias em processo de submissão continuada na Anvisa. A agência, então, está recebendo dados de cada etapa do estudo à medida em que elas são concluídas. O procedimento foi criado pelo governo federal para agilizar a análise de potenciais imunizantes contra a Covid-19.
Fontes-Dutra concorda que a submissão continuada é o modelo é o mais adequado para instruir a Anvisa sobre a viabilidade da Covaxin, considerando a avançada evolução da pandemia no país:
— Dada a situação que nos encontramos e nos encontraremos, a submissão da aprovação por uso emergencial é muito benéfica. Assim teremos o número suficiente de dados para já colocar uma vacina à disposição da população.
Procurada pelo GLOBO, a Anvisa informou que não recebeu informações das clínicas sobre a Covaxin.